Migração celular e metástase.
Créditos da imagem: Tabdanov et al, 2018.
Pesquisadores sabem há anos que os tumores apresentam padrões interiores, que são como pequenas “estradas” que as células cancerosas usam para se movimentar dentro dos tumores. Após atravessarem o tumor, elas caem nos vasos sanguíneos, tecidos adjacentes e assim, colonizam outra região fora do tumor primário. Pacientes que apresentam um alto número desses padrões em seus tumores têm menor chance de sobreviver ao câncer, já que o sucesso da célula sair do tumor e atingir o vaso sanguíneo é bem alto.
O que os pesquisadores não conseguiram descobrir até agora é como as células reconhecem esses padrões e se movem ao longo deles.
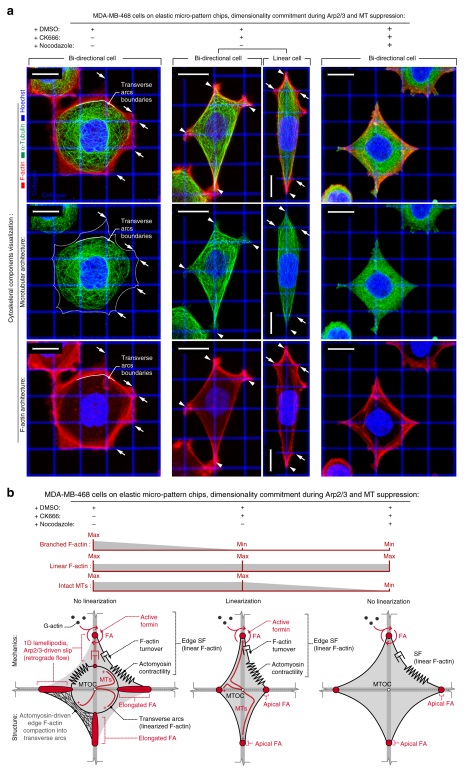
A orientação de contato devido à arquitetura de matriz extracelular é um regulador chave da invasão e metástase de carcinoma. Neste trabalho, usando uma plataforma com rigidez variável que facilita as indicações da matriz uniaxial ou biaxial, ou adesões competitivas da E-caderina, foi demonstrado distintos mecanismos de movimentação celular mediante a estímulo. Através da ruptura das forças de tração, observou-se uma profunda mudança fenotípica em direção a um modo de protrusão dendrítica e identificou-se processos bimodais que governam o sensoriamento de orientação. Em células contráteis, o sensoriamento de orientação é fortemente dependente de forminas e sinalização de FAK e pode ser perturbado pela ruptura da dinâmica dos microtúbulos, enquanto condições de baixa tração iniciam protrusões dendríticas do tipo fluídico que são dependentes de Arp2 / 3. A interrupção concomitante desses mecanismos bimodais anula completamente a resposta de orientação de contato. Assim, a detecção de orientação em células de carcinoma depende tanto da arquitetura ambiental quanto das propriedades mecânicas, e o direcionamento das respostas bimodais pode fornecer uma estratégia racional para interromper o comportamento metastático.
Veja o trabalho completo em anexo:
Bimodal sensing of guidance cues in mechanically distinct microenvironments
Keywords: #cellbiology; #cancerbiology; #cellmigration; #metastasis