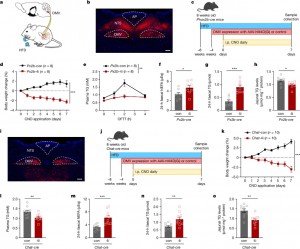
Absorção de gordura regulada por um circuito entre o cérebro e o intestino
Legenda: Legenda: a. Visão simplificada do caminho cérebro-tronco encefálico–nervo vago–intestino em camundongos alimentados com uma dieta rica em gorduras (HFD).
b. Neurônios positivos para PHOX2B no tronco encefálico de camundongos PHOX2B-Cre:Rosa26-tdTomato. AP, área postrema. c. Esquema do desenho experimental usando supressão quimiogenética da atividade do DMV em camundongos Phox2b-cre.
d–h. Mudanças observadas após a inativação de neurônios do DMV em camundongos Px2b-4i e Px2b-con (n = 8 por grupo). Alteração no peso corporal (d), níveis plasmáticos de TG após OFTTs (e), conteúdo de NEFA fecal em 24 h (f) e de TG (g), e níveis de TG no jejuno (h). i. Neurônios CHAT-positivos localizados no DMV de camundongos CHAT-Cre:Rosa26-tdTomato. j. Esquema do desenho experimental usando supressão quimiogenética da função do DMV em camundongos Chat-cre. k–o. Mudanças observadas após a inativação de neurônios do DMV em camundongos Chat-4i (n = 10 por grupo). Alteração no peso corporal (k), níveis plasmáticos de TG (l), conteúdo de NEFA fecal em 24 h (m) e de TG (n), e níveis de TG no jejuno (o). A coleta de amostras ocorreu no dia 7 após a aplicação de CNO. Amostras plasmáticas e do jejuno foram coletadas 2 h após a administração de 200 μl de óleo de oliva por gavagem. Barra de escala, 100 μm (b,i). Dados apresentados como média ± s.e.m. A significância foi avaliada usando análise de variância (ANOVA) de duas vias (d,e,k), teste t de Student bicaudal (f,g,l–o) ou teste de Mann–Whitney bicaudal (h). *P < 0,05, **P < 0,01, ***P < 0,001. Para estatísticas detalhadas, consulte os dados de origem.
Creditos da imagem: Lyu et a, 2024
Por muito tempo, acreditou-se que a absorção de gordura através da parede intestinal acontecia apenas por difusão passiva. No entanto, estudos recentes identificaram um circuito cérebro-intestino que regula a área de superfície dedicada à absorção de gordura. Um composto capaz de desativar esse circuito induziu perda de peso em camundongos, sugerindo que essa via pode ser um alvo promissor para o desenvolvimento de medicamentos contra a obesidade. O consumo excessivo de alimentos ricos em gordura ou com alta densidade calórica é um fator central no aumento global de obesidade e distúrbios metabólicos. Há mais de 160 anos, descobriu-se que o intestino delgado é o principal local onde ocorre a absorção de gordura. Este órgão evoluiu para ser altamente eficiente, com uma estrutura interna composta por vilosidades em forma de dedos e microvilosidades semelhantes a pelos, o que aumenta significativamente a superfície disponível para a absorção de nutrientes.
Tradicionalmente, considerava-se que a absorção de gordura era um processo passivo de difusão através das células epiteliais do intestino, sem envolvimento direto do sistema nervoso central. No entanto, algumas evidências sugerem que essa visão pode estar incompleta, e não está claro se a disfunção nas vias de comunicação cérebro-intestino contribui para o desenvolvimento da obesidade. Por isso, é crucial investigar como o cérebro pode influenciar a regulação da absorção de gordura no intestino. Descobrir esses mecanismos pode abrir portas para novas terapias no combate à obesidade e no manejo da saúde metabólica. Pesquisas demonstraram que o nervo vago, responsável pela comunicação bidirecional entre o cérebro e o intestino, desempenha um papel fundamental na regulação da absorção de gordura. Nos mamíferos, neurônios do núcleo motor dorsal do nervo vago (DMV), localizado no tronco cerebral, enviam projeções para várias partes do trato gastrointestinal. Utilizando uma técnica conhecida como quimiogenética, foi possível controlar a atividade dos neurônios do DMV que se conectam a diferentes regiões do intestino de camundongos, como o duodeno, jejuno e íleo. Surpreendentemente, a inativação dos neurônios do DMV que se projetam para o jejuno, mas não para outras áreas do intestino, resultou em uma redução significativa na absorção de gordura, o que também levou à perda de peso. A microscopia eletrônica mostrou que o desligamento desse circuito DMV–vago–jejuno reduziu o tamanho das microvilosidades no jejuno.
Em busca de compostos naturais que possam reduzir a atividade neuronal do DMV, um estudo avaliou diversos extratos em fatias de cérebro de camundongos. Entre os compostos analisados, a pueraria, extraída da raiz seca da videira *Pueraria lobata* (Willd.), usada há muito tempo na medicina tradicional chinesa, demonstrou um grande potencial. Análises posteriores identificaram que a pueraria se liga a receptores proteicos conhecidos como GABAA inibitórios, que possuem uma subunidade α1. Camundongos sem essa subunidade nos neurônios do nervo vago não apresentaram perda de peso ou diminuição das microvilosidades em resposta ao tratamento com pueraria. A microscopia eletrônica crioeletrônica foi usada para identificar o local exato de ligação da pueraria no receptor GABAA. Atualmente, o tratamento da obesidade frequentemente envolve procedimentos cirúrgicos que reduzem o tamanho do estômago ou desviam partes do intestino. No entanto, este estudo sugere que o encurtamento das microvilosidades no jejuno poderia reduzir a área de superfície disponível para a absorção de gordura, oferecendo uma alternativa potencial às cirurgias bariátricas para a perda de peso a longo prazo.
O orlistat, um medicamento aprovado pela FDA (Food and Drug Administration) dos Estados Unidos, impede que a enzima lipase quebre as moléculas de gordura, reduzindo assim sua absorção, mas pode causar efeitos colaterais como lesões no fígado. Ao contrário do orlistat, a pueraria age na via cérebro-intestino sem apresentar efeitos adversos conhecidos, podendo ser uma alternativa mais segura para limitar a absorção de gordura. No entanto, são necessários estudos clínicos adicionais para avaliar a eficácia terapêutica e os possíveis efeitos colaterais da pueraria em seres humanos.
A acetilcolina, um neurotransmissor liberado nas terminações do nervo vago, pode desempenhar um papel importante nesse circuito, talvez modulando proteínas que formam as microvilosidades. Pesquisas futuras serão necessárias para esclarecer os mecanismos de sinalização neuromodulatória envolvidos na comunicação entre o cérebro e o intestino e seus efeitos nas células epiteliais do jejuno.
Dietas ricas em gordura influenciam a atividade em regiões específicas do cérebro por meio de um eixo intestino-cérebro. Pesquisas adicionais são necessárias para entender como os sinais cerebrais relacionados a essas dietas são processados e transmitidos ao DMV. O mapeamento de subgrupos neuronais do DMV e sua relação com diferentes segmentos do intestino pode aprimorar nosso entendimento sobre o controle cerebral do metabolismo corporal.
A brain-to-gut signal controls intestinal fat absorption
A brain-to-gut signal controls intestinal fat absorption