A Senescência Hepática como Propagadora do Envelhecimento e Disfunção em Múltiplos Órgãos: Descobertas e Implicações para a Medicina Regenerativa
Legenda: A senescência hepatocelular resulta em senescência e disfunção em outros órgãos.
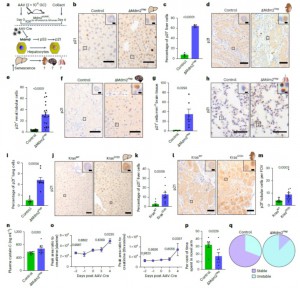
a, Um esquema do método experimental; camundongos Mdm2E5/E6fl; R26LSL-tdTomato/LSL-tdTomato de 8 a 12 semanas de idade foram injetados intravenosamente com 2 × 10¹¹ GC de AAV-Cre ou AAV-Null e sacrificados 4 dias depois. Os alvos a jusante de MDM2 são destacados.b, Imagens representativas de IHC para p21 em células hepáticas de camundongos ΔMdm2Hep e controle; n = 16/19 camundongos controle/ΔMdm2Hep, respectivamente.c, Quantificação automatizada de células hepáticas p21+; n = 4/5 camundongos controle/ΔMdm2Hep, respectivamente; teste t bicaudal não pareado.d, Imagens representativas de IHC para p21 em seções renais de camundongos.e, Quantificação manual de células tubulares renais p21+; os dados são apresentados por campo de visão (FOV), n = 16/19 camundongos controle/ΔMdm2Hep (controles adicionais mostrados na Figura de Dados Estendidos 1g); teste t de Welch bicaudal.f, Imagens representativas de IHC para p21 em seções cerebrais.g, Quantificação manual de células cerebrais p21+; n = 4/6 camundongos controle/ΔMdm2Hep, respectivamente; teste t de Welch bicaudal.h, Imagens representativas de IHC para p21 em seções pulmonares.i, Quantificação automatizada de células pulmonares p21+; n = 6/9 camundongos controle/ΔMdm2Hep, respectivamente; teste t bicaudal não pareado.j, Imagens representativas de IHC para p21 em seções hepáticas de camundongos KrasG12D/KrasWT.k, Quantificação automatizada de células hepáticas p21+; n = 8/11 camundongos KrasWT/KrasG12D, respectivamente; teste de Mann–Whitney bicaudal.l, Imagens representativas de IHC para p21 em seções renais de camundongos KrasG12D/KrasWT.m, Quantificação manual de células tubulares renais p21+; n = 14/16 camundongos KrasWT e KrasG12D, respectivamente; teste de Mann–Whitney bicaudal.n, Níveis plasmáticos de cistatina C em camundongos ΔMdm2Hep ou controle 4 dias após a injeção de AAV-Cre ou AAV-Null; n = 9/10 camundongos controle/ΔMdm2Hep, respectivamente; teste t de Welch bicaudal.o, Níveis urinários de alanina e treonina em camundongos ΔMdm2Hep antes e após a injeção de AAV-Cre; os pontos representam a área de pico média de n = 3/4/5 camundongos nos dias -2 e 0, 4 e -1 e 3, respectivamente; ANOVA de duas vias comparando cada ponto temporal ao dia de indução (dia 0).p, Proporção de tempo gasto pelos camundongos ΔMdm2Hep/controle no novo braço do labirinto em Y no dia 4; n = 7/9 camundongos controle/ΔMdm2Hep, respectivamente; teste t bicaudal não pareado.q, Proporção de oscilações estáveis versus instáveis em fatias do hipocampo; n = 13/14 fatias de cérebro de quatro camundongos controle/ΔMdm2Hep cada, respectivamente. Todas as barras representam a média ± erro padrão da média (s.e.m.), cada ponto representa uma amostra por camundongo, e os números são os valores de P. As barras de escala são de 50 μm e 5 μm nas ampliações dos insets. Os dados numéricos de origem estão disponíveis nos Dados de Origem.
Creditos da imagem: Kiourtis et al, 2024
A senescência celular é um estado de parada permanente do ciclo celular associado a uma série de processos fisiológicos e patológicos, como o envelhecimento, o desenvolvimento embrionário e a cicatrização. As células senescentes, além de cessarem sua proliferação, adotam um fenótipo secretor pró-inflamatório conhecido como SASP (fenótipo secretor associado à senescência), que libera fatores que afetam o ambiente celular ao redor. Um dos impactos mais graves da senescência ocorre no fígado, onde lesões severas podem levar a uma falência multiorgânica. No estudo liderado por Christos Kiourtis et al., publicado na Nature Cell Biology, os pesquisadores exploram o papel do fígado como um centro de propagação da senescência, investigando se a senescência hepática pode induzir um estado de envelhecimento celular em órgãos distantes, como rins, pulmões e cérebro.
Principais Descobertas
Utilizando modelos de camundongos e dados de pacientes com falência hepática aguda grave, o estudo mostrou que a senescência no fígado não apenas causa disfunção hepática, mas também promove senescência em outros órgãos, levando a falência multiorgânica. Em camundongos, a indução de senescência hepática foi realizada com a exclusão de um domínio específico do gene MDM2, que resultou em senescência celular nos hepatócitos, evidenciada pelo aumento na expressão do marcador de senescência p21 e pela atividade de β-galactosidase. Nos animais estudados, essa senescência se espalhou para os rins, cérebro e pulmões, induzindo um estado de disfunção nesses órgãos e afetando suas capacidades regenerativas.
O Papel Crítico da Via TGFβ
Uma descoberta central foi o papel da via de sinalização TGFβ como mediadora da propagação sistêmica da senescência. Os pesquisadores observaram que a presença de fatores associados ao SASP, principalmente TGFβ, era aumentada no plasma dos camundongos com senescência hepática. A exposição de órgãos distantes a esses fatores secretados pelo fígado resultou na ativação da via TGFβ, promovendo um estado de senescência nesses órgãos. Para testar a reversibilidade desse efeito, foi administrado um inibidor da via TGFβ, que bloqueou a propagação da senescência para os órgãos extra-hepáticos e preveniu a disfunção renal, cerebral e pulmonar induzida pela senescência hepática. Isso sugere que a via TGFβ desempenha um papel fundamental na transmissão endócrina da senescência.
Efeitos da Senescência no Cérebro e nos Rins
Além da disfunção hepática, os efeitos da senescência foram marcantes no cérebro e nos rins. No cérebro, camundongos com senescência hepática exibiram declínios cognitivos significativos, conforme indicado por uma redução na capacidade de explorar novos ambientes. Exames eletrofisiológicos em fatias de hipocampo revelaram oscilações anormais em resposta a estímulos, sinalizando comprometimento funcional. Nos rins, foi observado um aumento na expressão do marcador p21 e na atividade de β-galactosidase, que coincidiram com alterações metabólicas e na função de filtração renal. Marcadores de disfunção renal, como aumento nos níveis de creatinina e perda de aminoácidos na urina, foram observados, indicando que a senescência hepática impacta a capacidade de os rins manterem o equilíbrio de substâncias essenciais.
Estudos em Pacientes com Hepatite Aguda Grave
Para validar os achados em humanos, o estudo incluiu uma análise de pacientes com hepatite aguda grave de etiologia indeterminada, uma condição que frequentemente evolui para falência multiorgânica. Observou-se que os níveis de marcadores de senescência, como p21 e γH2AX, nas células hepáticas dos pacientes eram preditivos de desfechos clínicos, como a necessidade de transplante de fígado e a ocorrência de disfunções em outros órgãos. A presença elevada desses marcadores foi associada a um pior prognóstico e a um maior risco de falência multiorgânica. Esta correlação sugere que os marcadores de senescência hepática poderiam servir como indicadores precoces para o manejo de pacientes com falência hepática aguda.
Implicações Terapêuticas e Caminhos para o Futuro
Este estudo fornece evidências convincentes de que a senescência pode ser transmitida entre órgãos, promovendo disfunções multiorgânicas em resposta a uma senescência primária em um órgão específico, neste caso, o fígado. As descobertas ressaltam o potencial de estratégias terapêuticas que bloqueiem a via TGFβ como forma de interromper a transmissão sistêmica da senescência, o que poderia melhorar a sobrevida e a qualidade de vida de pacientes com doenças graves do fígado e reduzir o risco de falência multiorgânica. Além disso, os pesquisadores sugerem que tratamentos baseados em senolíticos (substâncias que eliminam células senescentes) ou senomórficos (que modificam o fenótipo senescente) podem ser explorados para combater os efeitos deletérios da senescência nos órgãos distantes.
Em suma, esta pesquisa lança luz sobre o papel sistêmico da senescência hepática e sugere que a interrupção da via TGFβ pode ser uma abordagem promissora para a medicina regenerativa e para o tratamento de falência multiorgânica associada à senescência.
Hepatocellular senescence induces multi-organ senescence and dysfunction via TGFβ
Hepatocellular senescence induces multi-organ senescence and dysfunction via TGFβ