PAGER: Uma Nova Fronteira para Programar o Comportamento Celular com Receptores Sintéticos
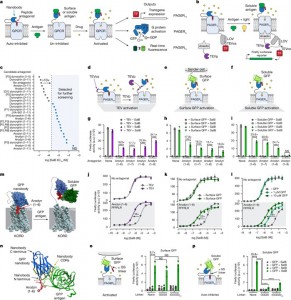
Legenda: a. Visão Geral do PAGER.** A auto-inibição pelo antagonista peptídico fundido é aliviada pela ligação ao antígeno, permitindo a ativação do GPCR por uma droga. A ativação do PAGER pode dirigir a expressão de transgenes (PAGERTF), ativação de proteínas G (PAGERG) ou fluorescência em tempo real (PAGERFL). TF, fator de transcrição. b. Esquema do PAGERTF.** A expressão de transgenes dirigida pelo PAGER baseia-se no SPARK (ferramenta de associação de proteínas específicas que fornece leitura transcricional com cinética rápida). A ativação do PAGERTF resulta na liberação proteolítica de um fator de transcrição ancorado. LOV, domínio sensível a luz, oxigênio e voltagem. c. Resumo dos valores de EC50 do SalB para os peptídeos antagonistas candidatos testados no PAGERTF.** *n* = 3 experimentos independentes, 3 réplicas por condição. ND, não definido. d–f. Esquemas para a ativação do PAGERTF** por TEVp extracelular (d), GFP expresso na superfície (e) ou GFP solúvel (f). g–i. Atividade do PAGERTF em resposta ao tratamento com SalB e TEVp (g), co-cultivo com células HEK apresentando GFP na superfície (h) ou GFP solúvel (i). *n* = 3, 5 ou 4 experimentos independentes, respectivamente, 3 réplicas por condição. Dados são média ± desvio padrão. Teste ANOVA de duas vias com comparação múltipla de Tukey. a.u., unidades de absorbância. j–l. Curvas de dose-resposta do SalB** para a atividade do PAGERTF com antagonista arodyn (1–6) e pré-tratamento com TEVp (j), co-cultivo com células HEK apresentando GFP na superfície (k) ou GFP solúvel (l). *n* = 5, 2 ou 2 experimentos independentes, respectivamente, 3 réplicas por condição. Dados são média ± desvio padrão. m. Modelo AlphaFold2** de antagonismo e alívio dependente de antígeno no PAGER. PM, membrana plasmática. n. Modelo AlphaFold2** destacando a proximidade entre as CDRs (amarelo) e o N-terminal do nanocorpo, onde o peptídeo antagonista (vermelho) está fundido. o. Variantes PAGERTF com linkers flexíveis Gly-Ser** podem ser ativadas por GFP de superfície expresso em células HEK 293T co-cultivadas. *n* = 3 experimentos independentes, 3 réplicas por condição. Dados são média ± desvio padrão (ANOVA de duas vias com comparações múltiplas de Tukey). p. Variantes PAGERTF com linkers flexíveis Gly-Ser** não podem ser ativadas por GFP solúvel. *n* = 3 experimentos independentes, 3 réplicas por condição. Dados são média ± desvio padrão. Teste ANOVA de duas vias com comparações múltiplas de Tukey. *P* < 0,05, **P** < 0,01, ***P*** < 0,001, ****P**** < 0,0001; NS, não significativo.
Creditos da imagem: Kalogriopoulos et al, 2024
Cientistas da Universidade de Stanford e da Universidade de Pequim apresentaram uma tecnologia revolucionária publicada na revista Nature. Trata-se dos PAGERs (Programable Antigen-Gated G-protein-coupled Engineered Receptors), uma nova classe de receptores acoplados à proteína G (GPCRs) sintéticos. Esses receptores têm a capacidade de interpretar sinais extracelulares, definidos por antígenos específicos, para controlar uma ampla variedade de respostas celulares. Essa abordagem inovadora supera limitações de tecnologias anteriores, como receptores de antígenos quiméricos (CARs) e receptores sintéticos Notch, ao introduzir uma maior modularidade e flexibilidade no design dos receptores.
Os PAGERs são baseados em um conceito de auto-inibição condicional. O sistema utiliza nanocorpos (fragmentos de anticorpos altamente específicos) para detectar antígenos-alvo. Quando um antígeno se liga ao nanocorpo, ele desativa um domínio inibitório acoplado ao GPCR, permitindo que o receptor seja ativado por uma droga específica. Essa ativação controla uma série de processos celulares que podem incluir a expressão de genes, emissão de fluorescência em tempo real ou ativação de vias de sinalização naturais. Essa adaptabilidade faz dos PAGERs ferramentas incrivelmente versáteis, permitindo aplicações em pesquisa básica e translacional.
Principais Avanços e Aplicações
Controle da Migração Celular
Um dos experimentos demonstrou que os PAGERs podem ser usados para guiar células T ao longo de gradientes de antígenos solúveis. Essa funcionalidade é particularmente importante no contexto do tratamento de tumores, onde a dificuldade de infiltração de células T em tecidos sólidos é um desafio crítico para imunoterapias.
Diferenciação de Macrófagos
Os pesquisadores também mostraram que os PAGERs podem modular a diferenciação de macrófagos, induzindo a conversão de células imunológicas para estados pró-inflamatórios ou anti-inflamatórios dependendo do sinal recebido. Essa capacidade pode ser utilizada para influenciar respostas imunológicas em ambientes tumorais ou inflamatórios.
Produção de Biomoléculas Terapêuticas
Em outra aplicação, os PAGERs foram usados para desencadear a liberação de anticorpos terapêuticos em resposta à detecção de antígenos tumorais. Isso inclui a produção de anticorpos bi-específicos que direcionam células T para destruir células cancerígenas específicas.
Modulação da Atividade Neuronal
A tecnologia também foi empregada para regular a atividade de neurônios em camundongos. Dependendo do antígeno-alvo, os PAGERs foram capazes de ativar ou silenciar neurônios em fatias de cérebro. Essa aplicação demonstra o potencial do sistema para estudos de circuitos neurais e para o desenvolvimento de novas terapias para distúrbios neurológicos.
Design Modular e Impacto Futuro
O diferencial mais significativo dos PAGERs é sua modularidade. Alterar o nanocorpo no receptor permite direcioná-lo a novos antígenos de forma relativamente simples, o que possibilita sua aplicação a uma ampla gama de moléculas, desde proteínas virais até fatores de crescimento e receptores de superfície celular. Essa abordagem reduz significativamente o tempo e os recursos necessários para desenvolver novos receptores, em comparação com métodos tradicionais de evolução dirigida ou mutagênese estrutural.
Além disso, o design dos PAGERs permite controle temporal rigoroso por meio de drogas específicas, aumentando a precisão e minimizando possíveis efeitos adversos. Os pesquisadores destacam que os PAGERs podem ser combinados com outras tecnologias baseadas em GPCRs, como sensores fluorescentes e circuitos genéticos programáveis, para criar sistemas ainda mais sofisticados.
Conclusão
Os PAGERs representam uma nova fronteira na bioengenharia, permitindo a criação de células sintéticas capazes de responder a estímulos extracelulares de maneira controlada e programável. Sua capacidade de integrar sinais complexos e gerar respostas diversificadas os torna ferramentas poderosas tanto para pesquisa quanto para aplicações terapêuticas, desde o tratamento de doenças como câncer e distúrbios neurológicos até a modulação de respostas imunológicas. Com um potencial tão amplo, os PAGERs têm o potencial de revolucionar a biologia celular e a medicina de precisão nos próximos anos.
Synthetic GPCRs for programmable sensing and control of cell behaviour-compressed
Synthetic GPCRs for programmable sensing and control of cell behaviour